¿Cómo medimos el Volumen de un Cóctel?
Para medir el volumen de un cóctel nos basaremos en diferentes formulas, pero antes debemos conocer los conceptos que estaremos tratando: Solución es la suma de un soluto más un solvente, nosotros lo tenemos en nuestro día a día cuando preparamos siropes. La fórmula para este cálculo es la siguiente:
Vsol: Vsto + Vste y la traducimos así (Vsol: Vsoluto + V solvente = Vsolución)
Ejemplo 1: Vsol: 30 g azúcar (Vsto) + 70 ml agua (Vste) = 300 ml (Vsol)
¿Qué es un soluto y solvente?
Soluto: Es la sustancia que se disuelve, siempre se encuentra en menor proporción ya sea expresada en peso o volumen.
Solvente: Es la sustancia que disuelve al soluto generalmente se encuentra en mayor proporción. “El Solvente universal es el agua (H20) esto se debe a su alta polaridad.
Solución: Es el resultado final de la combinación del soluto y el solvente.
Ejercicio 2:
¿Cuál es el % en volumen de 50 ml de Ron a (40% GL) en 5 ml de agua?
Para conocer el porcentaje de alcohol primero debemos calcular el volumen de al solución (volumen del cóctel) ya que la fórmula para el porcentaje de alcohol es: % OH : Vsto / Vsol x 100 (volumen de soluto divido entre el volumen de solución multiplicado por 100).
Datos:
Incógnita: % v-OH = ?
Paso I:

Calculamos el Vsol: 50 ml (Vsto) + 5ml (Vste) = (Vsol = 55ml)
Paso II:

Calculamos el % = (50 ml / 55 ml) x 100 = 0.909 x 100 = % 90,90
Conclusión final:
El resultado muestra que la solución está a 90,90 % de su valor inicial, si lo multiplicamos por los 40% GL del Ron veremos que se diluye a 36,36 % GL lo que quiere decir que ha perdido 9,1% GL.
Debemos quedarnos con este ejemplo porque lo veremos más adelante.
¿Cuál es la densidad del agua (H2O)?
La cantidad de masa (m) por unidad de volumen (v) es el concepto que manejaremos para la densidad (D) y se representa con la letra griega (Ro) para nuestros defectos y facilitar los post lo representamos la letra (D).
Como describimos en los artículos anteriores, para calcular la densidad dividimos la masa sobre el volumen. D: m / v
Este ejercicio lo vimos lo representamos así:
1ml = 1 cm3 (un mililitro ml es igual a un centímetro cubico cm3)
1.000ml = 1.000 cm3
1.000ml = 1 L (litro) = 1.000 cm3 (se puede decir que mil mililitros es igual a un litro de agua y este es igual a mil centímetros cúbicos). El agua así como los líquidos pueden cambiar su forma (masa) pero mantienen su volumen.
Ejemplo:
Si colocamos 1 L de liquido (agua) en una botella cilíndrica esta adquiere la forma del cilíndrica, pero si lo colocamos en un recipiente cuadrada con la misma capacidad de volumen este adquiere forma cuadrada cambiando su masa por con el mismo volumen. La única marera de que pierda volumen es que el recipiente tenga una capacidad de volumen más pequeña.
Ya que tocamos el tema de líquidos no podemos dejar pasar la Mecánica de Fluidos.
Mecánica de Fluidos termino que está presente en el bar en muchos ejemplos pero el más común es la flotabilidad del hielo o la decoración en nuestros cócteles, para ellos debemos conocer el Principio de Arquímedes que dice:
“Todo cuerpo sumergido total o parcial en un fluido, experimenta un empuje o fuerza de flotación igual al peso del volumen desalojado del fluido”.
Lo expresamos así:
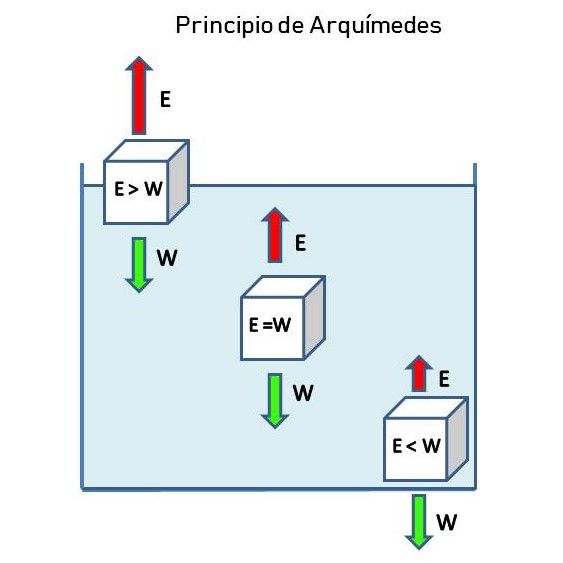
E > W (cuando el empuje (E) es mayor al peso (W) del cuerpo este flota).
E = W (cuando el empuje es igual al peso del cuerpo se mantiene en flotabilidad dentro del fluido).
E < W (cuando el empuje es menor al peso del cuerpo este se hunde hasta el fondo).
Empuje (E): Es la fuerza hacia arriba que se genera para expulsar el cuerpo se mide en Newton.
Peso (W): Es la fuerza con la que la tierra atrae a un cuerpo se mide en Newtons /m3 la fuerza de gravedad equivalencia constante es de 9,8 m/s2 (metros sobre segundo cuadrado). Calculamos el peso con esta fórmula; W= m (masa) x gravedad (9,8).
¿Qué es el Coeficiente de Solubilidad?
Coeficiente de solubilidad es el límite de soluto agregado al solvente a una temperatura dada para formar una solución saturada, este varía según las condiciones y puede aumentar o disminuir a medida que cambia la temperatura y el soluto.
Existe un límite en la capacidad de disolución del disolvente.
Ejemplo:
Si colocamos azúcar en un vaso de agua a temperatura ambiente al principio, notará que el azúcar desaparece en el agua. Sin embargo, si se continúa agregando azúcar, encontraremos que en algún momento comenzará a acumularse en el fondo del vaso.
Esto se debe a que el agua, que es el solvente, ha alcanzado su límite de solubilidad. y la cantidad máxima de concentración. El soluto que permanece en el fondo del recipiente y no se disuelve se llama “Cuerpo Inferior”.
Ahora si tenemos el mismo vaso con agua caliente el coeficiente de solubilidad aumenta, ya que las moléculas del agua están más activas y reaccionan con el soluto para una mejor dilución o integración, caso contrario si tenemos el mismo vaso pero con agua fría, el proceso de dilución es más lento.
Las soluciones se pueden clasificar por cantidad de soluto disuelto. Por lo tanto, pueden ser de tres tipos: saturados, insaturados y sobresaturados.
Solución Saturada: La solución ha alcanzado el límite del coeficiente de solubilidad, es decir, hay una cantidad máxima de soluto disuelto en el solvente a una temperatura dada.
Solución no Saturada: La cantidad de soluto disuelto aún no ha alcanzado el coeficiente de solubilidad. Eso significa que se puede agregar más soluto.
Solución Supersaturada: Hay más soluto disuelto que en condiciones normales. En este caso se ha precipitado el solvente.
¿El hielo cuando se derrite desplaza por su volumen al volumen de un líquido?
La respuesta es No, el hielo ocupa su espacio de volumen dentro de la unidad y al diluirse solo cambia de estado sólido a liquido manteniendo el volumen ocupado.
Cuando preparamos un coctel debemos tener en cuenta que siempre colocamos el hielo primero y seguido el coctel o sus ingredientes, la suma de estos nos da el volumen que deseamos en la bebida, lo explicaremos mas adelante con un ejemplo.
Se preguntaran porque después que preparamos un trago y le agregamos mas hielo el trago puede derramar o sube de nivel (esto es una técnica muy usada para completar el cóctel cuando nos quedamos cortos). Esto se debe al grado inicial de dilución del hielo, lo que usualmente sucede en este caso es que al agregar hielo sin considerar su volumen excedemos el volumen total de capacidad de la cristalería.
Ejemplo: Preparamos un MAI TAI en un vaso corto, lo primero que hacemos es agregar el hielo seguido la mezcla de ingredientes si tenemos experiencia podemos quedar exactos en la medida final, pero imaginemos quedemos cortos y para compensar esto agregamos hielo, si no lo hacemos con razonamiento corremos el riesgo de derramar la mezcla o peor sobre poner hielo y al pasar unos segundo comienza a derretir y desbordar la bebida. Esto se debe que hemos excedido el volumen que se puede contener en el vaso.
Sucede mucho con aquellos bartenders que tienen la genialidad de completar los cócteles con hielo granizado o pile. Es muy importante tener claros cuales son las capacidades de nuestra cristalería así mismo los volúmenes de los cocteles, tiempo inicial de dilución del hielo y cantidades de ingredientes, haciendo un simple cálculo nunca podremos cometer este error.

En una nueva publicación presentaremos nuestras practicas y conclusiones de los experimentos realizados en diferentes técnicas de coctelería y sustituiremos algunos términos adaptándolos a la coctelería como (Volumen de Solución = Volumen del cóctel), Solvente (licor base o modificadores), Soluto (modificadores) entre otros.


